Druhy řešení. Typy koncentrace roztoku
Roztoky jsou homogenní hmoty sestávající ze dvou nebo více látek nebo směsi, ve kterých jedna látka působí jako rozpouštědlo a druhá jako rozpustné částice.
Existují dvě teorie interpretace původuroztoky: Chemická, který je zakladatelem DI Mendělejev, a fyzické, navržené německým a švýcarským fyzikem Ostwald a Arrhenius. Podle výkladu Mendeleev, rozpouštědlo a rozpuštěné složky se stávají účastníky chemické reakce za vzniku těkavých sloučenin těchto stejných prvků nebo částic.
Fyzická teorie popírá chemikálieinterakce mezi molekulami rozpouštědla a rozpuštěných látek, což vysvětluje proces vzniku kapalin jako rovnoměrné rozdělení částic (molekuly, ionty) mezi částicemi rozpouštědla rozpouští látku v důsledku fyzikálních jevů nazývaných difúze.
Klasifikace řešení podle různých kritérií
V současné době neexistuje jednotný systém klasifikace řešení však podmíněné typy řešení lze rozdělit na nejdůležitějších kritérií, a to:
I) Podle souhrnného stavu jsou izolovány pevné, plynné a kapalné roztoky.
II) Velikost částic rozpuštěné látky: koloidní a pravdivá.
III) Stupeň koncentrace částic rozpuštěné látky v roztoku: nasycený, nenasycený, koncentrovaný, zředěný.
IV) Schopností provádět elektrický proud: elektrolyty a neelektrolyty.
V) Účel a použití: chemické, lékařské, konstrukční, speciální řešení atd.
Druhy řešení podle souhrnného stavu
Klasifikace řešení agregátním stavemrozpouštědla obsažená v širokém smyslu slova hodnot. To je považováno za řešení kapalná látka (a jako rozpuštěné látky mohou působit jako kapalné nebo pevné prvku), ale s ohledem na skutečnost, že řešení - homogenní systém skládající se ze dvou nebo více sloučenin, je logické rozpoznat i pevné roztoky, a plynné. Tuhé roztoky se považuje směs, např. Několik kovů, známý hovorově jako slitiny. Plynné druh řešení - směs několika plynů, příklad - okolní vzduch nás, který je reprezentován jako směs kyslíku, dusíku a oxidu uhličitého.
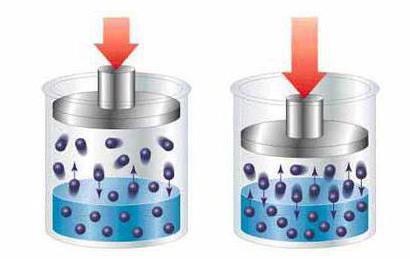
Roztoky podle velikosti rozpuštěných částic
Typy roztoků podle velikosti rozpuštěných částiczahrnují pravé (konvenční) roztoky a koloidní systémy. V pravých řešeních se rozpustná látka rozkládá na malé molekuly nebo atomy, které jsou přibližně velikosti molekul rozpouštědla. V tomto případě zachovávají původní typy rozpouštědel původní vlastnosti rozpouštědla, jen nepatrně je přeměňují pod působením fyzikálně-chemických vlastností prvku, který se k němu přidává. Například: při rozpouštění stolní soli nebo cukru ve vodě zůstává voda ve stejném stavu agregace a stejné konzistence, prakticky stejné barvy, mění se pouze její chuť.

Koloidní roztoky se liší od obvyklých roztoků,že přidaná složka se nerozkládá úplně, zachovává komplexní molekuly a sloučeniny, jejichž rozměry značně přesahují částice rozpouštědla, přesahující hodnotu 1 nanometru.
Typy koncentrace roztoku
Při stejném množství rozpouštědla lze přidat jiné množství rozpouštěcího prvku, na výpustě budou mít roztoky s různými koncentracemi. Uvádíme hlavní z nich:
- Nasycené roztoky se vyznačují stupněmrozpustnost látky, při které složka rozpuštěná látka pod vlivem konstantní teplotě a tlaku je již rozpadá na atomy a molekulami, a roztok dosáhne rovnovážné fáze. Nasycené roztoky mohou být také rozděleny do koncentrátů, v nichž hmotnostní podíl rozpuštěných složek je srovnatelná s rozpouštědlem a zředí kde rozpuštěná látka je několikanásobně méně rozpouštědla.
- Nenasycené - to jsou roztoky, ve kterých se rozpuštěná látka může stále rozpadat na malé částice.
- Přesycené roztoky se získají, kdyžparametry ovlivňujících faktorů (teplota, tlak), v důsledku čehož pokračuje proces "rozdrcení" rozpuštěné látky, stane se větší než v normálních (obvyklých) podmínkách.
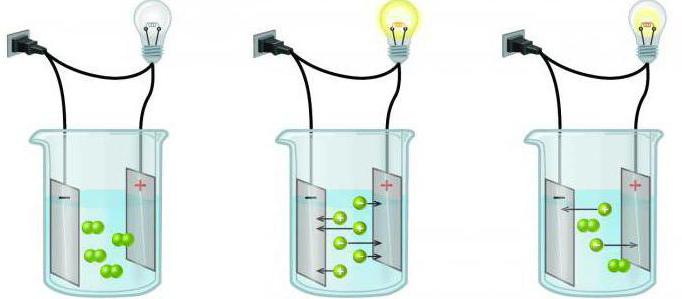
Elektrolyty a neelektrolyty
Některé látky v roztoku se rozkládajíionty schopné provádět elektrický proud. Takové homogenní systémy se nazývají elektrolyty. Tato skupina zahrnuje kyseliny, většinu solí. A řešení, která nevedou elektrický proud, se obvykle nazývají neelektrolyty (téměř všechny organické sloučeniny).
Skupiny řešení podle účelu
Řešení jsou nepostradatelná ve všech odvětvích národního hospodářství, jejichž specifika vytvořila takové typy speciálních řešení, jako jsou zdravotnické, stavební, chemické a další.
Lékařská řešení jsou kolekcípřípravky ve formě mastí, suspenzí, šťáv, roztoky pro infuzi a vstřikování, a jiných lékových forem používaných pro lékařské účely pro léčení a prevenci různých onemocnění.

Typy chemických řešení zahrnujíobrovský počet homogenních sloučenin používaných v chemických reakcích: kyseliny, soli. Tyto roztoky mohou být organického nebo anorganického původu, vodné (mořské vody) nebo bezvodé (na bázi benzenu, acetonu atd.), Kapalné (vodky) nebo tuhé (mosazné). Našly uplatnění v různých odvětvích národního hospodářství: v chemickém, potravinářském a textilním průmyslu.
Typy malty se liší viskózní a hustou konzistencí, protože jsou vhodnější pro název směsi.








