Co je OVR v moderní chemii?
Promluvme si o tom, co je OVR v anorganické a organické syntéze.
Definice procesu
Redoxové reakce zahrnují takové procesy, které povedou ke změně stupně oxidace ve dvou nebo více chemických prvcích v komplexních nebo jednoduchých látkách.

Co je to oxidace?
Oxidací se rozumí taková chemikáliereakce, při které atom nebo specifický iont vydává elektrony, přičemž snižuje počáteční oxidační stav. Tento proces je typický pro kovy.
Co je zotavení?
Tím se rozumí proces restaurováníchemická transformace, která povede ke snížení stupně oxidace v iontu nebo jednoduché látce s přídavkem elektronů. Tato reakce je charakteristická pro nekovové a kyselé zbytky.
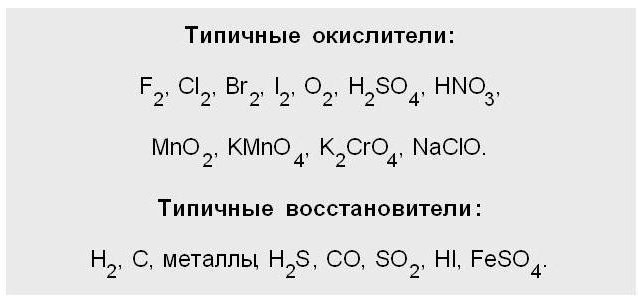
Charakteristika redukčního činidla
Vzhledem k tomu, co je OVR, nemůžeme tento pojem ignorovat jako "reduktivní".
Tím se rozumí neutrální molekula nebonabitý iont, který jako výsledek chemické interakce poskytne jiný ion nebo atom elektronu, přičemž zvyšuje stupeň oxidace.

Stanovení oxidačního činidla
Argumentovat nad tím, co je OVR je také důležitézmínit také termín, jako je "oxidant". Tímto způsobem je zvykem znamenat takové ionty nebo neutrální atomy, které během chemické interakce budou mít záporné elektrony z jiných atomů nebo neutrálních částic. Současně se sníží původní oxidační stav.
Typy OBR
Pokud jde o to, co je OVR, je třeba si uvědomit ty odrůdy těchto procesů, které jsou nejčastěji zvažovány v anorganické a organické syntéze.
Intermolekulární interakce předpokládají takovéprocesy, ve kterých jsou atomy jak redukčního činidla, tak oxidačního činidla umístěny v různých výchozích materiálech, které vstupují do interakce. Příkladem tohoto typu transformace je interakce mezi oxidem manganičitým (4) a kyselinou chlorovodíkovou, což vede k plynnému chloru, dvojmocnému chloridu manganatému a vodě.
V tomto chemickém procesu, jakochlorové anionty se při interakci objevují oxidující. Kation manganu (s oxidačním stavem +4) vykazuje v reakci oxidativní schopnosti při zachování dvou elektronů.
Intramolekulární interakce jetakové chemické konverzní nichž alespoň atomů a redukčního činidla a oxidačního činidla, jsou na počátku alespoň jedním výchozí látky a po konverzi jsou v různých reakčních produktů.
Jako příklad tohoto typu reakce,představují rozklad chlorečnanu draselného. Po zahřátí se tato látka změní na chlorid draselný a kyslík. Oxidační vlastnosti budou charakteristické pro chlorečnanový anion, který při odebírání pěti elektronů v reakci bude redukován na chlorid.
V tomto případě se kyslíkový anion projevíredukující vlastnosti, oxidace na molekulární kyslík. Co je v tomto případě OVR? Jedná se o proces přenosu elektronů mezi ionty, což vede k tvorbě dvou reakčních produktů.
Také pro tento typ chemické transformace,vyskytující se se změnou stupně oxidace prvků původně nalezených v jednom vzorci, je proces rozkladu dusičnanu amonného. Dusík, který stojí v amoniovém kationtu a má stupeň oxidace -3, během procesu dává šest elektronů a oxiduje na molekulární dusík. A tento dusík, který je součástí nitritu, vezme šest elektronů, zatímco jde o redukční činidlo, a během reakce je oxidován.
Co je OVR v chemii? Výše uvedená definice ukazuje, že jde o transformace spojené se změnami v několika prvcích oxidačních stavů.
Self-oxidace a redukce (disproporcionální)předpokládá takové procesy, při nichž jako redukční činidlo a oxidační činidlo existuje jeden počáteční atom, který se zvýší a současně sníží jeho oxidační stav po dokončení interakce. Pokud jde o to, co je OVR v chemii, příklady takových transformací lze nalézt i v průběhu chemie na střední škole. Rozklad siřičitanu draselného při zahřívání vede k tvorbě dvou solí tohoto kovu: sulfidu a síranu. Síra s oxidačním stavem +4 vykazuje jak redukční, tak oxidační vlastnosti, zvyšuje a snižuje oxidační stav.

Abychom pochopili, co znamená OVI v chemii, pojďme to nazvatjiný typ takových chemických přeměn. Kontrproportsionirovanie zahrnuje takové procesy, v důsledku kterého oxidační a redukční činidlo atomy jsou složeny z různých výchozích složek, ale na pravé straně, tvoří reakční produkt. Například tím, že se nechá reagovat oxid síry (4) se sirovodíkem za vzniku síry a vody. Ion síry v oxidačním stavu +4 bude mít čtyři elektrony, a síra iont s indikátorem -2 ztrácí dva elektrony. Výsledkem je, že oba se mění na jednoduchou látku, ve které je stupeň oxidace nulový.

Závěr
Vzhledem k otázce toho, co je OVR v chemii,poznamenáváme, že to jsou četné transformace, které fungují živé organismy, dochází k různým přírodním procesům a jevům. Za účelem uspořádání koeficientů v těchto rovnicích je nutné sestavit elektronickou rovnováhu.






