Schéma železo-uhlík. Schéma stavu systému železa a uhlíku
Je těžké si představit moderní stavbu,strojů, strojů a dalších důležitých odvětvích bez použití hlavních kovových slitin z oceli a litiny. Jejich výroba převyšuje všechny desítky časů.
Pokud uvažujeme ocel a litinu z hlediskataková věda jako věda o kovu, centrální postava je schéma stavu slitin železa a uhlíku, což nám umožňuje získat podrobné náměty o složení a strukturálních přeměnách v těchto materiálech. A také seznámit se s jejich fázovým složením.
Historie objevu
Poprvé, když v slitinách (ocelí a litých žehličkách)existují jisté (zvláštní) body, poukázal na velký metalurg a vynálezce - Dmitrij Konstantinovič Černov (1868). Byl to ten, kdo učinil důležitý objev o polymorfních transformacích a je jedním z tvůrců schématu stavu železa a uhlíku. Podle Černova je pozice těchto bodů na diagramu přímo závislá na procentu uhlíku.
A co je nejzajímavější, je od okamžiku tohoto objevu, že taková věda jako metalografie začíná svůj život.
Schéma slitin železa s uhlíkem je výsledkem ustálené práce vědců z několika zemí světa. Všechna abecední označení hlavních bodů a fází v diagramu jsou mezinárodní.
Koncept schématu
Grafické znázornění procesů probíhajících v roce 2008slitina se změnou teplotního režimu, koncentrace látek, tlak, se nazývá stavový diagram. Umožňuje vizuálně a vizuálně zobrazit všechny transformace vyskytující se ve slitinách.
Prvky diagramu železo-uhlík
Stručné informace o každém z těchto prvků.
Železo je stříbřitě šedý kov. Specifická hmotnost - 7, 86 g / cm3. Má teplotu tání 1539 ° C.
Když se železo a jiné kovy vzájemně ovlivňují, vytvářejí se sloučeniny nazvané substituční roztoky. Pokud s nekovy, například s uhlíkem nebo vodíkem, pak - řešení implantace.
Železo má schopnost, původněsolidní, být v několika státech, které v metalurgii je obvyklé nazývat "alfa" a "gamma". Tato kvalita se nazývá polymorfismus. O tom později v článku.
Uhlík je nekovový. Pokud se objeví jako grafit, pak je teplota tání 3500 ° C. Je-li oba diamant 5000 ° C. Hustota uhlíku je 2,5 g / cm3. Má také polymorfní vlastnosti.
V slitinách železa a uhlíku tvoří tento prvek pevný roztok, jehož složení je ferrum nazývaný cementite (Fe3C). Také tvoří grafit v litině.
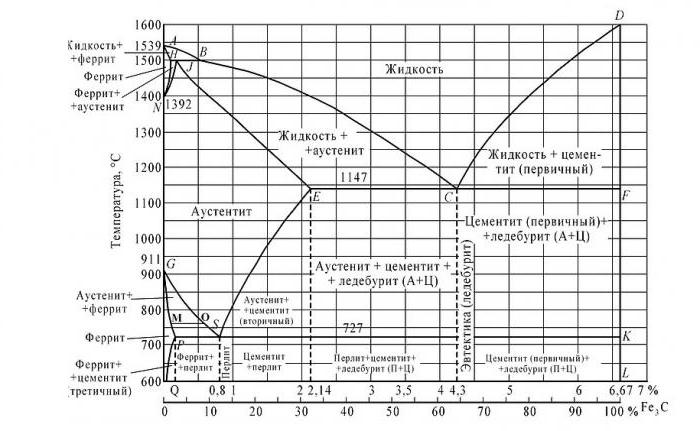
Schéma slitiny železa a uhlíku
Výsledkem vzájemného působení vzájemných diagramů je získání cementitu - chemické sloučeniny.
Zpravidla se při studiu schématu od studentů kovů považují všechny stabilní vazby za součásti a samotný grafický obraz se zkoumá částečně.
Také ve třídě je na schématu železa a uhlíku vykreslena chladicí křivka: je vybráno procento uhlíku a pak je nutné určit, která fáze odpovídá teplotě v diagramu.
K tomu, kromě samotného diagramunakreslit souřadný systém (teplota-čas). Počínaje maximálním stupněm, postupujte postupně směrem dolů a zobrazte křivku a části přechodu z jedné fáze do druhé. V tomto případě je nutné je volat a označit typ krystalové mřížky.
Dále uvažujme podrobněji grafické znázornění diagramu stavu železa a uhlíku.
Nejprve má dvě formy (části):
- železo-cementit;
- železo-grafit.
Za druhé, slitiny, ve kterých jsou hlavními "herci" ferrum a uhlík, jsou obvykle rozděleny do:
- oceli;
- žehličky.
V případě, že uhlíku ve slitině je menší než nebo rovno 2,14% (bod E ve schématu) této oceli, je-li více než 2,14% - železo. Z tohoto důvodu je diagram rozdělen do dvou fází.
Polymorfní transformace
Více o každé fázi o něco později v článku. Stručně řečeno, realizace hlavních transformací nastává při specifických teplotách.
Stav železa je označen jako α-ferrum (při teplotě nižší než 911 ° C). Křišťálová mřížka je objemová krychle orientovaná na obličej. Nebo BCC. Vzdálenost mezi atomy takové mřížky je poměrně vysoká.
Železo získá gama modifikaci, tj. Označuje jako γ-ferrum (911-1392 ° C). Křišťálová mřížka je tvář-centrovaná kostka (fcc). V této mřížce je vzdálenost mezi atomy nižší než v bcc.
Když α-ferrum projde do γ-ferrumu, objem hmotyse zmenší. Důvodem je krystalová mřížka - její forma. Protože fcc mřížka má více uspořádaný stav atomů než bcc.

Pokud se přechod uskutečňuje v opačném směru - od γ-ferrumu k α-ferrumu, zvyšuje se objem slitiny.
Když teplota dosáhne 1392 ° C (aleméně než je teplota tání železa 1539 ° C), pak se α-ferruum přemění na δ-ferrum, ale není to jeho nová forma, ale pouze odrůda. Navíc, δ-ferrum je nestabilní struktura.
Vlastnosti technicky čistého železa
Magnetické vlastnosti železa při různých teplotách:
- méně než 768 ° C - feromagnetický;
- více než 768 ° C - paramagnetické.
Teplotní bod 768 ° C se nazývá magnetický konverzní bod nebo bod Curie.
Vlastnosti technicky čistého železa:
- tvrdost - 80 HB;
- dočasný odpor 250 MPa;
- mez kluzu - 120 MPa;
- prodloužení o 50%;
- relativní zúžení - 80%;
- vysoký modul pružnosti.

Karbid ze železa
Grafický pohled na součást diagramu železo-uhlík: Fe3C. Látka se nazývá karbid železa nebo cement. Je charakterizován:
- Obsah uhlíku je 6,67%.
- Specifická hmotnost je 7,82%.
- Křišťálová mřížka má kosočtvercový tvar, skládající se z oktaedru.
- Tavení se provádí při teplotě asi 1260 ° C
- Nízké feromagnetické vlastnosti při nízkých teplotách.
- Tvrdost je 800 HB.
- Plasticita je prakticky nulová.
- Karbid železa tvoří pevné roztokysubstituce, ve kterých jsou atomy uhlíku jsou nahrazeny atomy nekovů (dusíku), a atomů železa - kovy (chrom, wolfram, mangan). Tato pevná konstrukce názvem dopované.
Jak bylo uvedeno výše, cementite jenestabilní fáze a stabilní grafit. Vzhledem k tomu, že první látka je nestabilní sloučenina, rozkládá se za určitých teplotních podmínek.

Ve schématu železo-uhlík existují takové stavy:
- kapalná fáze;
- ferit;
- austenit;
- cementite;
- grafit;
- perlit;
- ledeburite.
Každou z nich uvažujme podrobně.
Kapalná fáze
Ferrum v kapalném stavu dobře rozpouští uhlík. To je bez ohledu na to, do jaké míry jsou v procentech. V důsledku toho se vytvoří homogenní kapalná hmota.
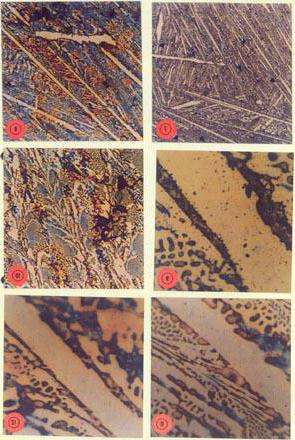
Ferit
Je pevným roztokem zabudování uhlíku doα-ferrum. Může být také zahrnuto malé množství nečistot. Ale ferit má téměř stejné vlastnosti jako čisté železo. Pokud budeme uvažovat o struktuře pod mikroskopem, uvidíme polyhedrální zrnky světelného tónu.
Stává se to:
- při nízké teplotě (při teplotě 727 ° C, 0,02% uhlíku, rozpustnost);
- Vysoká teplota (při 1499 ° C rozpustnost uhlíku je 0,1%), nebo se nazývá δ-ferrum.
Vlastnosti feritu:
- tvrdost - 80-120 HB;
- dočasný odpor 300 MPa;
- prodloužení je 50%;
- má dobré magnetické vlastnosti (až do teploty 768 ° C).
Austenit
Jedná se o pevný roztok inkorporace uhlíku vγ-ferrum. Může také existovat malé množství nečistot. V krystalové mřížce je uhlík ve středu fcc buňky. Při zvážení struktury austenitu pod mikroskopem je vidět jako lehká zrna polyhedrálního tvaru s dvojčaty.
Má následující charakteristiky:
- Rozpustnost uhlíku v γ-ferrumu je 2,14% (při teplotě 1147 ° C).
- Tvrdost austenitu 180 HB;
- Prodloužení - 40-50%;
- Dobré paramagnetické vlastnosti.
Cementite a jeho formy
Prezentace v těchto fázích: C 1, C 2, C 3 (primární, sekundární a terciární cementit).
Pokud jde o fyzikálně-chemické parametry těchto tří stavů, jsou přibližně stejné. Mechanické vlastnosti jsou ovlivněny velikostí částic, jejich počtem a polohou.
Podle diagramu je také zřejmé, že:
- U1 je tvořen z kapalného stavu (pod mikroskopem je viděn jako velká deska);
- Z2 - z austenitu (usazování kolem jeho zrna ve formě mřížky);
- C3 - z feritu (nachází se na hranicích feritových zrn ve formě jemných částic).
Perlit a ledeburite
Směs feritu a cemenitu se nazývá perlit. Vzniká při rozkladu austenitu (při teplotě nižší než 727 ° C). Při zvětšení má tato struktura tvar desek nebo zrn.
Perlit s postupným poklesem teploty je přítomen ve všech slitinách s obsahem uhlíku 0,02-6,67%.
Ledeburite je směs austenitu a cementu. Vzniká z kapalné fáze po ochlazení na teplotu pod 1147 ° C.
Litina
Slitiny ve schématu železo-uhlík, kterýobsahují uhlík více než 2,14%, se nazývají litiny. Jsou velmi křehké. Průřez takového litého železa má světelný tón, a proto se nazývá bílé železo.
V diagramu je to bod C, nazvaný eutektický,s odpovídajícím obsahem uhlíku 4,3%. Během krystalizace se vytvoří směs tvořená austenitem a cementitem, společně nazývaným ledeburite. Fázové složení je konstantní.

Při koncentraci uhlíku menší než 4,3%(pre-eutektická litina) během krystalizace, austenit je uvolněn z roztoku. Pak z něj je přidělen Ts2. A při 727 ° C se austenit změní na perlit. Strukturální stav takového litého železa je následující: velké plochy tmavého perlitu.
V hypereutektické bílé litině (více uhlíku4,3%) po ochlazení probíhá strukturování při tvorbě krystalů CI. Další transformace jsou již provedeny v pevném stavu. Struktura je ledeburite, což je pozadí pro tmavé perlitové pole. A velké vrstvy jsou CI.

Závěry
Není možné dosáhnout absolutní rovnováhy, fyzikální i chemické, s výjimkou speciálních laboratorních podmínek.
V praxi lze rovnováhu přiblížitAbsolutní, ale za určitých podmínek: dostatečně pomalé zvýšení nebo snížení teploty slitiny, které bude trvat dlouhou dobu.





